Anthropogene Einträge von Calcium:
- Calciumchlorid als Abfallprodukt der chemischen Industrie und des Bergbaus
- Calciumchlorid im winterlichen Straßendienst
Durch folgende Reaktionen kann Calcium in Lösung gehen:
- Eintrag von CO2-haltigem Wasser (z.B. saurer Regen) führt zur Auflösung von Calciumcarbonat und Calciumsulfat
- Eintrag von Salpetersäure als Folge der Nitrifikation von Stickstoffverbindungen bei der Düngung führt ebenfalls zur Auflösung. Bei niedrigen pH-Werten werden auch Tonminerale und Silikate aufgelöst, an denen Calcium gebunden war, welches somit ins Grundwasser gelangt.1,2
Calcium ist ein essenzielles Element für Knochen und Zähne.
Daher haben die im Trinkwasser vorkommenden Konzentrationen für einen gesunden Menschen positive gesundheitliche Auswirkungen.
Seit 2001 wird auf eine Regelung einer Calciumkonzentration in der Trinkwasserverordnung vollständig verzichtet.
Calcium ist für Menschen, Tiere und Pflanzen essenziell. Im menschlichen Körper befinden sich etwa 15 g Calcium pro Kilogramm Körpergewicht, wobei der Großteil in den Knochen gespeichert ist.
Calcium im Trinkwasser ist generell förderlich für die Gesundheit. Es unterstützt die Mineralstoffversorgung des Körpers und spielt eine entscheidende Rolle bei der Entwicklung und dem Erhalt von Knochen und Zähnen sowie bei der Blutgerinnung, der Muskelfunktion und der Weiterleitung von Nervensignalen. Ein Calciummangel kann gesundheitliche Probleme wie Osteoporose begünstigen. Allerdings sollte beachtet werden, dass sehr hartes Wasser mit hohen Calciumkonzentrationen Verkalkungen in Rohrleitungen und Haushaltsgeräten verursachen kann.3
Viele Mineralwässer werben mit einem idealen 2:1-Verhältnis von Calcium zu Magnesium, doch was bedeutet das?
In genau diesem Verhältnis kann Ihr Körper beide Mineralstoffe optimal aus dem Wasser aufnehmen.
So unterstützen Sie Ihre Gesundheit auf natürliche Weise – mit jedem Schluck!4

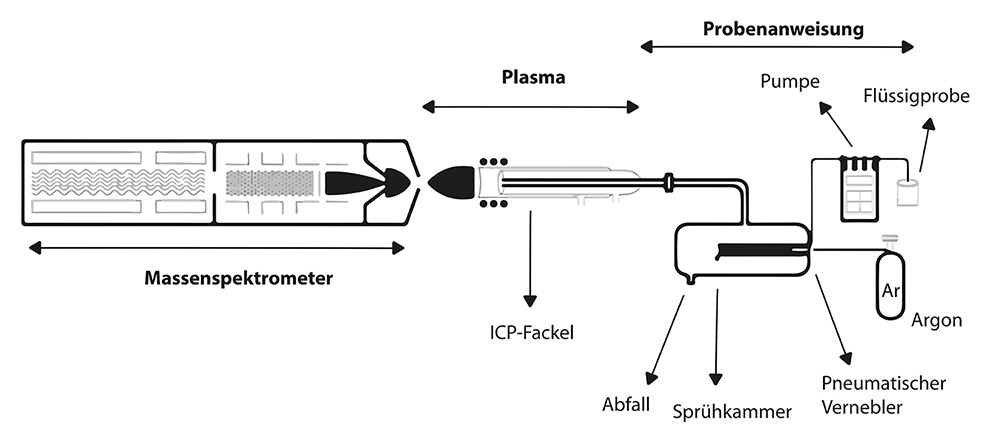
Die ICP-MS-Technik zeichnet sich durch ihre schnelle und kostengünstige Analyse aus.
Eine weitere verwandte Methode ist die ICP-OES-Technik, bei der induktiv gekoppeltes Plasma mit optischer Emissionsspektrometrie kombiniert wird. Hierbei wird die Probe durch Argonplasma angeregt. Diese Technik eignet sich besonders zur Bestimmung von Schwermetallen, insbesondere in Sedimenten, Gesteinen und industriellen Abfällen.6
Wie kann ich eine Wasserprobe im Labor beauftragen?
Verweise
1 Vgl. Grundwasserbeschaffenheit - LfU Bayern. (Abgerufen am 12.03.2025).
2 Vgl. W. Kölle: Wasseranalysen – richtig beurteilt, 2010, Wiley-VCH.
3 Vgl. Calcium | Nds. Ministerium für Umwelt, Energie und Klimaschutz (niedersachsen.de). (Abgerufen am 12.03.2025).
4 Vgl. Trinkwasser, Mineralwasser, Tafelwasser – was sind die Unterschiede? | Verbraucherzentrale.de. (Abgerufen am 12.03.2025).
5 Vgl. W. Kölle: Wasseranalysen – richtig beurteilt, 2010, Wiley-VCH.
6 Vgl. Element (ICP-OES und ICP-MS) Bestimmung - EUROLAB (laboratuvar.com). (Abgerufen am 12.03.2025).