Das chemische Element Kalium (Elementsymbol: K) gehört wie Natrium zu der Gruppe der Alkalimetalle. In Reinform ist Kalium ein silbergraues, weiches Metall mit einer sehr hohen Reaktionsfreudigkeit. Aufgrund dieser kommt Kalium in der Natur nur in Form von Verbindungen vor.
Kalium kann auf verschiedene Weise in Oberflächengewässer, Grundwasser und somit auch in Leitungs- bzw. Brunnenwasser gelangen:
Geogene Eintragswege von Kalium:
-
Auswaschungen von Kaliumchlorid oder Kaliumsulfat aus Salzlagerstätten
-
Auswaschungen von Kaliumaluminiumsilikat aus den gesteinsbildenden Mineralien Feldspat und Glimmer
Anthropogene Eintragswege von Kalium:
-
Kalium ist in Abwässern des Kalibergbaus zu finden, wo Abraumsalze wie Sylvin (KCl) und Carnallit (KMgCl₃ * 6 H₂O) abgebaut werden.
-
Kaliumsalze spielen eine wichtige Rolle bei der landwirtschaftlichen Düngung.


Durch folgende Reaktionen kann Kalium im Wasser gelöst werden:
- Eintrag von CO2-haltigem Wasser (z. B. saurer Regen) führt zur Auflösung von
Kaliumchlorid oder Kaliumsulfat.
- Eintrag von Salpetersäure als Folge der Nitrifikation von Stickstoffverbindungen bei der
Düngung führt ebenfalls zur Auflösung. Bei niedrigen pH-Werten werden auch Tonminerale
und Silikate aufgelöst an denen Kalium gebunden war, welches somit ins Grundwasser
gelangt.1,2
Kalium ist für Menschen, Tiere und Pflanzen unverzichtbar. Kalium trägt zur Aufrechterhaltung des osmotischen Drucks, des Elektrolytgleichgewichts und des Säure-Basen-Haushalts bei. Es spielt außerdem eine wichtige Rolle bei der Weiterleitung von Nervenimpulsen und ist entscheidend für Muskelkontraktionen, die Herzfunktion und die Regulierung des Blutdrucks. Ein Kaliummangel kann unter anderem bei starkem Flüssigkeitsverlust, etwa durch Durchfall, auftreten.3, 4
Die geschätzte angemessene Kaliumzufuhr für Erwachsene liegt laut Deutscher Gesellschaft für Ernährung (DGE) bei ca. 4 g täglich.4
Der Beitrag des Trinkwassers zur Kaliumversorgung ist in der Regel unbedeutend, weshalb ein Grenzwert bei der Bestimmung der Wasserqualität für Kalium weder toxikologisch noch ernährungsphysiologisch erforderlich ist. Daher existiert für Kalium seit 2001 in der TrinkwV (Trinkwasserverordnung) auch kein Grenzwert mehr.3, 4
👉 Kaliumsalze sind in der landwirtschaftlichen Düngung von großer Bedeutung.
👉 Tonmineralien binden Kalium stark. Ein Problem kann entstehen, wenn Kalium in größere
Bodentiefen vordringt, insbesondere wenn:
- der Boden nur geringe Mengen an Tonmineralien enthält.
- landwirtschaftliche Flächen über lange Zeit intensiv genutzt wurden, sodass das Speichervermögen der Tonminerale erschöpft ist.
👉Auf Sandböden kann es je nach Sickerwassermenge zu Kaliumauswaschungen von
20 bis 50 kg/ha kommen. Bei einer Grundwasserneubildung von 220 mm/a würden sich daraus Kaliumkonzentrationen von 9,1 bis 22,7 mg/l im frisch gebildeten Grundwasser ergeben.
👉Erhöhte Kaliumkonzentrationen im Grundwasser treten auf, wenn Säuren durch kaliumhaltige Tonminerale neutralisiert werden, vor allem bei Abwesenheit von Kalk und niedrigen pH-Werten.
👉Ist der Kaliumgehalt in der Wasseranalyse des Grundwassers höher als der Nitratgehalt, so weist dies auf besondere geochemische Verhältnisse oder auf fäkale Verunreinigungen hin.
Seit 1980 wurde der Einsatz mineralischer Kalidüngemittel in der Landwirtschaft Deutschlands von 91,1 um ca. zwei Drittel auf 27,4 kg K/ha reduziert!
In der Folge haben die Gehalte an pflanzenverfügbarem Kalium im Boden in Ackerbauregionen deutlich abgenommen.5,6
Um Kalium in der Wasserprobe zu bestimmen, sind folgende Analyseverfahren möglich:
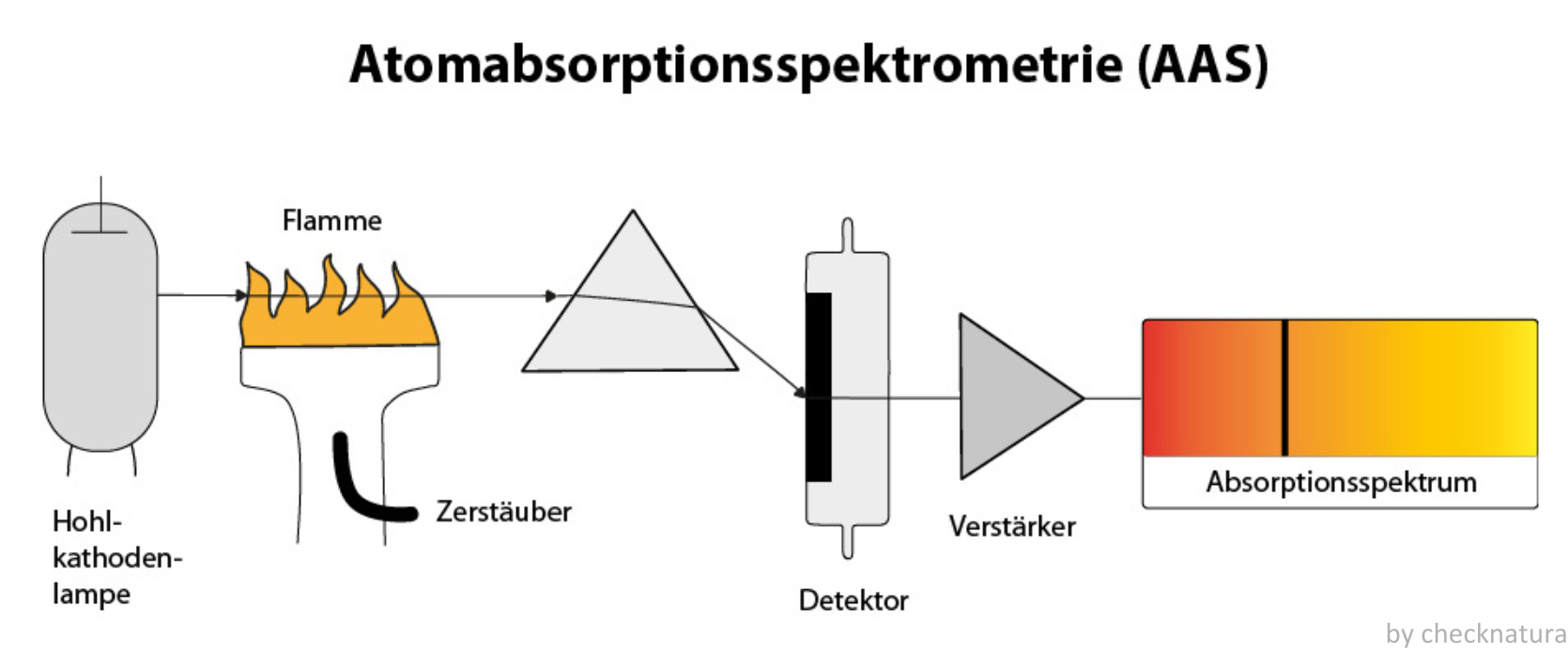
Die Atomabsorptionsspektrometrie (AAS) ist eine leistungsstarke analytische Methode zur quantitativen und qualitativen Bestimmung von Metallen und Halbmetallen in Proben. Beim AAS-Verfahren trifft die von einer Lichtquelle erzeugte Strahlung auf die atomisierten Bestandteile der Probe und wird dabei teilweise absorbiert. In der Regel wird als Lichtquelle eine Hohlkathodenlampe verwendet, deren Kathode aus dem zu analysierenden Element besteht. Das untersuchte Element absorbiert Strahlung auf einer für dieses charakteristischen Wellenlänge, was zu einer Abschwächung der Strahlungsintensität führt.7
Ionenchromatographie
Die Ionenchromatographie ist ein Trennverfahren, mit dem geladene Moleküle in einem Stoffgemisch erkannt und gemessen werden können. Bei der Ionenchromatographie wird eine mobile Phase durch das System gepumpt. Die zu analysierende Probe wird in das System injiziert und gelangt in die Trennsäule oder Ionenaustauschersäule, welche aus Materialien wie Quarzglas, Epoxidharzen oder Polyetheretherketon besteht. Ein Detektor identifiziert die Inhaltsstoffe der Probe und misst ihre Mengen.8,9
Schadstoffe oder Keime im Trinkwasser? Wie kann ich eine Wasserprobe im Labor beauftragen?
Bei zentraler Wasserversorgung wird eine einwandfreie Trinkwasserqualität von den Wasserversorgern nur bis zum Hausanschluss garantiert. Auf den letzten Metern bis zur Entnahme kann das Leitungswasser allerdings mitunter durch Komponenten der Hausinstallation wie Rohrleitungen und Boiler mit zum Beispiel Schwermetallen belastet werden. Auch ein Eintrag von Keimen ist durch die Hausinstallation in seltenen Fällen möglich. Zur Überprüfung der Leitungswasserqualität bieten wir deshalb verschiedenste Trinkwassertests an.
Betreiber von eigenen Brunnen sind für die Qualität und gesundheitliche Unbedenklichkeit des gewonnenen Brunnenwassers selbst verantwortlich. Wie Sie eine Wasseranalyse Ihres Brunnenwassers zur Eigenkontrolle oder durch einen geschulten Probenehmer (rechtssichere Wasseranalyse) beauftragen können, erfahren Sie hier:

Wie kann ich eine Wasserprobe im Labor beauftragen?
Verweise
1Vgl.: Kölle, W.: Wasseranalysen – richtig beurteilt, Wiley-VCH, 2010.
2Vgl.: Bayerisches Landesamt für Umwelt (LfU): Grundwasserbeschaffenheit, abrufbar unter: https://www.lfu.bayern.de/wasser/grundwasserbeschaffenheit. (Abgerufen am 12.03.2025).
3Vgl.: Niedersächsisches Ministerium für Umwelt, Energie und Klimaschutz: Kalium, abrufbar unter: https://www.umwelt.niedersachsen.de/startseite/themen/wasser/grundwasser/grundwasserbericht_niedersachsen/grundwasserbeschaffenheit/guteparameter/grundprogramm_des_nlwkn/kalium/Kalium-137600.html.
4Vgl.: Deutsche Gesellschaft für Ernährung (DGE): Kalium, abrufbar unter: https://www.dge.de/wissenschaft/referenzwerte/kalium/. (Abgerufen am 12.03.2025).
5Vgl.: Kölle, W.: Wasseranalysen – richtig beurteilt, Wiley-VCH, 2010.
6Vgl.: Bayerisches Landesamt für Umwelt (LfU): Grundwasserbeschaffenheit, abrufbar unter: https://www.lfu.bayern.de/wasser/grundwasserbeschaffenheit. (Abgerufen am 12.03.2025).
7Vgl.: Chemie.de: Atomspektroskopie, abrufbar unter: https://www.chemie.de/lexikon/Atomspektroskopie.html. (Abgerufen am 12.03.2025).
8Vgl.: Carl Roth GmbH: Ionenchromatographie einfach erklärt, abrufbar unter: https://www.carlroth.com/de/de/ionenchromatographie. (Abgerufen am 12.03.2025).
9Vgl.: Kölle, W.: Wasseranalysen – richtig beurteilt, Wiley-VCH, 2010.